2.7 Modelo atómico actual: modelo mecano-cuántico
O modelo de Rutherford seguía sen explicar moitos fenómenos físicos importantes, como por exemplo os espectros atómicos da maioría dos elemento químicos. Tampouco puido facelo o modelo proposto polo físico dinamarqués Niehls Bohr un pouco máis tarde (é un modelo parecido ao de Rutherford, pero os electróns só poden xirar nunhas cantas órbitas permitidas). Cumpriu modificar estes modelos, nacendo deste xeito, a principios do século XX, unha nova disciplina dentro da Física: a mecánica cuántica. Dada a dificultade desta disciplina describiremos moi brevemente como é o modelo que propón.
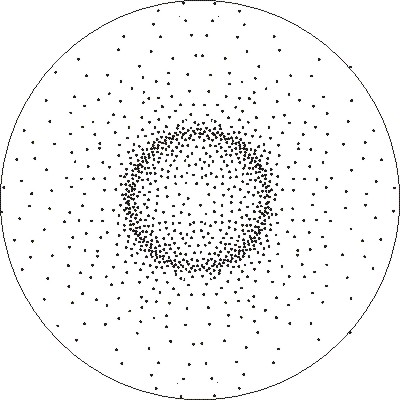
O núcleo segue concentrando a carga positiva do átomo pero xa non se fala de órbitas definidas para o electrón, senón de orbitais. Un orbital defínese como a zona do espazo onde hai maior probabilidade de atopar o electrón. Esta maior probabilidade indícase no debuxo con puntos e alí onde hai maior probabilidade haberá máis puntos. No debuxo vemos claramente que atoparemos con maior probabilidade o electrón preto do núcleo.
Actividade proposta
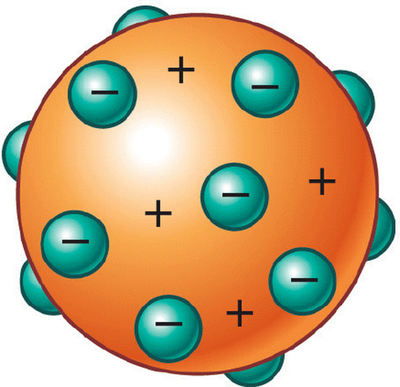
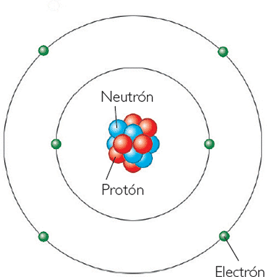
S10. Relaciona os distintos debuxos do átomo co nome correcto do modelo.
Licenciado baixo a Licenza Creative Commons Recoñecemento Non-comercial Compartir igual 3.0