2.2.1 Variación da presión dun gas co seu volume
Podemos investigar como varía a presión se metemos gas (vale o aire) dentro dun recipiente cun émbolo móbil (como o pistón no motor dun coche ou unha xiringa) conectado a un manómetro, mantendo constante a temperatura.
 |
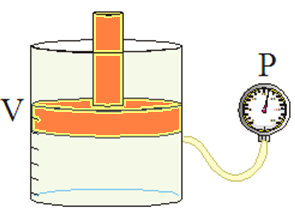 |
Imos cambiando o volume do gas á medida que prememos o émbolo; para cada volume anotamos a presión que indica o manómetro. Nunha experiencia obtivéronse os resultados seguintes:

Lei de Boyle
Xa vemos que canto maior é a presión menor é o volume: son inversamente proporcionais. Hai unha relación matemática entre volume e presión, coñecida como lei de Boyle:
Por Educaplus baixo licenza CC By-NC-ND
|
P.V = constante Tamén expresada como: P 1V 1 = P 2V 2 |
Pódeo comprobar vostede cos datos da táboa anterior. Multiplicando o volume pola presión, ha observar que sempre dá o mesmo resultado: iso é o que quere dicir "constante".
Actividades resoltas
Os gases no pistón dun motor ocupan 1,05 litros estando a 1 atm de presión. O émbolo comprime os gases ata reducir o seu volume á cuarta parte do inicial. Cal é a presión dos gases agora se non variou a temperatura?
| Solución |
Como a temperatura non cambia, podemos aplicar a lei de Boyle:
A presión faise catro veces maior que a inicial. |
Licenciado baixo a Licenza Creative Commons Recoñecemento Non-comercial Compartir igual 3.0