2.15.1 Propiedades dos metais
-
Poden ser elementos puros ou mesturas de varios metais (aliaxes).
-
Son sólidos a temperatura ambiente, aínda que hai uns poucos líquidos, como o mercurio.
-
Son bos condutores da calor e da electricidade, debido á doada mobilidade dos electróns pola rede metálica.
-
Disólvense ben con outros metais cando están fundidos.
-
A rede cristalina metálica pode deformarse e facer láminas (maleabilidade) ou fíos (ductilidade), e non son fráxiles.
Actividades resoltas
Que tipo de enlace (iónico, covalente ou metálico) se formará entre as parellas de elementos seguintes: Fe-Al, Li-Cl, O-N, C-C, Na-Na, H-Ne?
| Fe- Al | Metálico (son dous metais) | C-C | Covalente (son non metais) | |
| Li-Cl | Iónico | Na-Na | Metálico | |
| O- N | Covalente | H-Ne | Covalente |
Cando se xuntan metais diferentes forman aliaxes e non compostos. Por que?
| Solución | Os compostos teñen fórmulas fixas, como CO2 (dous átomos de osíxeno por cada un de carbono). Nas aliaxes a proporción entre os dous metais que se enlazan pode ser moi variable, non ten que ser fixa. Realmente son máis unha disolución que un composto en sentido estrito. |
Actividades propostas
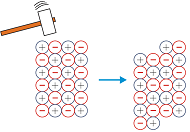
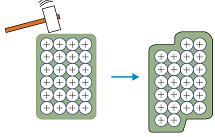
S25. As redes cristalinas do enlace iónico son fráxiles, non poden deformarse sen romper. Pero as metálicas si. Por que? Axúdese observando as figuras:
|
|
|
| Un golpe na rede iónica... | ... e outro na rede metálica. |
Licenciado baixo a Licenza Creative Commons Recoñecemento Non-comercial Compartir igual 3.0