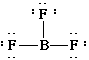2.14.1 Propiedades das substancias covalentes moleculares
-
Teñen temperaturas de fusión e ebulición baixas, son gases ou líquidos a temperatura ambiente. Isto é debido a que as forzas de atracción entre moléculas son débiles, así que costa pouco traballo separalas.
-
Non conducen ben a electricidade.
-
Son pouco solubles en xeral en auga, e bastante solubles en disolventes orgánicos.
Actividades resoltas
Que tipo de enlace hai nas substancias seguintes?
| CO2 | Covalente, xa que o carbono e o osíxeno son non metais. |
| C2H6 | Covalente: o carbono e o hidróxeno son non metais. |
| O2 | Covalente: os dous átomos de osíxeno que se enlazan son non metais. |
| SrI2 | Iónico: o estroncio (Sr) é metal, o iodo (I) é non metal. |
Represente os diagramas de lewis da seguintes molécula HF e BF3
| HF | BF3 |
|
|
|
Actividades propostas
S21. Represente os diagramas de Lewis das moléculas: SH2 e PH3.
S22. O iodo, I2, ten un enlace covalente. Diga cal será a súa solubilidade (grande ou pequena) en auga, alcohol e gasolina.
S23. A parafina é unha substancia covalente derivada do petróleo. Fundirá a temperatura alta ou baixa?
S24. Para formar unha molécula covalente, cantos átomos de flúor se xuntan cun de nitróxeno?
Licenciado baixo a Licenza Creative Commons Recoñecemento Non-comercial Compartir igual 3.0